Lungenembolie

Einleitung
Bei der Behandlung einer Lungenembolie kommen gerinnungshemmende Medikamente zum Einsatz. Sie verringern das Risiko für einen schweren Verlauf. Als Nebenwirkung können Blutungen auftreten.
Gerinnungshemmer sind Medikamente, die dafür sorgen, dass es länger dauert als normal, bis das Blut gerinnt. Sie werden eingesetzt, um zu verhindern, dass ein Blutgerinnsel wächst und weitere Gerinnsel entstehen. Außerdem unterstützen sie den Körper dabei, Gerinnsel zu verkleinern und aufzulösen. Abhängig vom Risiko werden die Mittel auch über eine längere Zeit angewendet, um zukünftige Gerinnsel zu verhindern und damit einer erneuten Lungenembolie vorzubeugen.
Der medizinische Fachbegriff für Gerinnungshemmer lautet Antikoagulanzien, die gerinnungshemmende Behandlung wird als Antikoagulation bezeichnet.
Symptome
Typische Anzeichen einer Lungenembolie sind:
- plötzliche schwere Atemnot
- Brustschmerzen
- Husten, vor allem mit blutigem Auswurf oder zusammen mit anderen Symptomen einer Lungenembolie
- Schwindel oder Benommenheit bis hin zur Ohnmacht
- Herzrasen
- starkes Angstgefühl
Bei diesen Beschwerden sind häufig ein oder mehrere größere Lungengefäße blockiert.
Einige Menschen mit Lungenembolie haben keine oder nur leichte Symptome.
Am Anfang hatte ich nur leichte Rückenschmerzen und dachte, ich hätte mir etwas ausgerenkt. Später konnte ich nicht mehr liegen, weil ich keine Luft bekam, und ich schwitzte stark.
Ursachen
Die meisten Lungenembolien sind die Folge einer Venenthrombose. Dabei bildet sich ein Blutgerinnsel in einer Vene. Wenn es ganz oder teilweise mit dem Blutstrom in Richtung des Herzens weggeschwemmt wird und eine Lungenarterie oder ihre kleineren Äste blockiert, kommt es zu einer Lungenembolie.
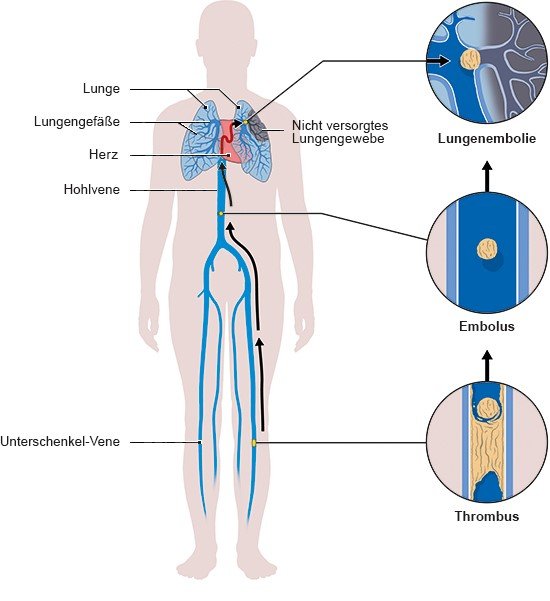
Die meisten Thrombosen entstehen in einer Bein- oder Beckenvene. Das Risiko für eine Lungenembolie ist höher, wenn sich das Blutgerinnsel im Oberschenkel oder im Becken bildet oder starke Beschwerden verursacht.
Sehr selten wird eine Lungenembolie durch eine andere Ursache ausgelöst. Dann verstopfen zum Beispiel eine Luftblase oder ein Fremdkörper eine Lungenarterie.
Risikofaktoren
Allgemein gilt: Risikofaktoren für eine Venenthrombose erhöhen auch das Risiko für eine Lungenembolie. Besonders hoch ist das Risiko, wenn mehrere Faktoren zusammenkommen. Die wichtigsten Risikofaktoren sind:
- Knochenbruch der Hüfte oder des Beins
- größere Operationen, zum Beispiel der Einsatz eines künstlichen Knie- oder Hüftgelenks
- Blutgerinnungsstörung, zum Beispiel das Antiphospholipid-Syndrom
- eine frühere Thrombose
- Krebserkrankungen wie Magen-, Lungen- und Blutkrebs oder ein Hirntumor
- eine Herzerkrankung wie Herzschwäche, Herzinfarkt oder Vorhofflimmern
- Hormonbehandlung in den Wechseljahren
- Verhütung mit hormonellen Verhütungsmitteln, die auch das Hormon Östrogen enthalten (wie die meisten Antibabypillen)
Weitere Risikofaktoren, die für sich allein genommen das Risiko für eine Lungenembolie nur leicht erhöhen, sind unter anderem:
- hohes Alter
- Schwangerschaft
- Übergewicht
- Bluthochdruck
- Diabetes mellitus
- Krampfadern
- Bettruhe von mehr als drei Tagen (Immobilität)
- Infektionen der Lunge, zum Beispiel eine Covid-19-Infektion
Häufigkeit
Das Risiko für eine Lungenembolie steigt im Laufe des Lebens: Im Alter zwischen 40 und 50 Jahren erkranken pro Jahr etwa 1 von 1000 Menschen daran, ab 80 Jahren etwa 10 von 1000.
Männer sind insgesamt häufiger betroffen als Frauen. Allerdings bekommen Frauen unter 45 und ab 80 Jahren öfter eine Lungenembolie als Männer in diesem Alter. Jüngere Frauen haben ein etwas höheres Risiko durch hormonelle Verhütungsmittel und während einer Schwangerschaft.
Verlauf
Wie eine Lungenembolie verläuft, hängt von der Größe und Anzahl der Blutgerinnsel in der Lunge ab. Außerdem spielt der allgemeine Gesundheitszustand eine Rolle – insbesondere, wie gut Herz und Lunge arbeiten.
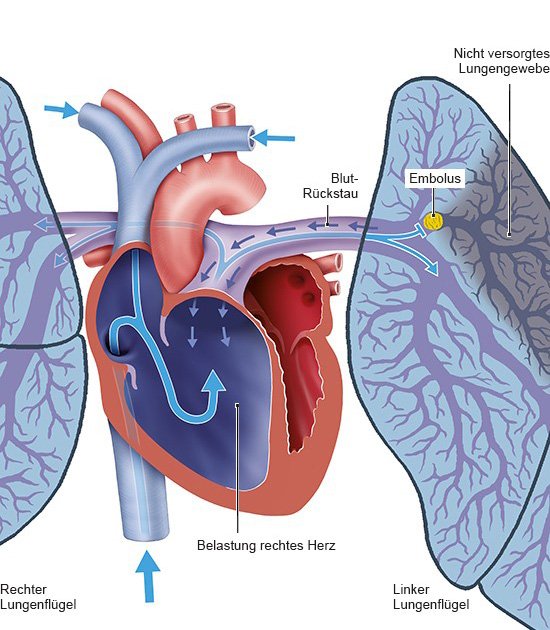
Meist gelingt es dem Herzen, gegen den Gefäßverschluss in der Lunge anzupumpen. Ist das Herz jedoch beispielsweise durch eine Erkrankung geschwächt, kann es nicht genug Blut in die Lunge pumpen, sodass der Blutdruck sinkt. Wenn der Körper nicht mehr ausreichend mit Sauerstoff versorgt wird, droht ein Kreislaufversagen.
Der Blutdruck während der Lungenembolie ist daher ein guter Indikator für ihren Verlauf: Von 100 Personen mit Lungenembolie haben
- etwa 95 einen ausreichenden Blutdruck. Sie haben insgesamt ein geringes Risiko für einen schweren oder tödlichen Verlauf.
- etwa 5 einen viel zu niedrigen Blutdruck. Sie haben ein hohes Risiko für einen schweren oder tödlichen Verlauf.
Vor allem bei anhaltenden Risikofaktoren wie einer Krebserkrankung oder Blutgerinnungsstörung sind auch weitere Embolien möglich.
Folgen
Viele Menschen haben noch Monate nach der Lungenembolie Atembeschwerden oder sind körperlich weniger belastbar. Dieser Zustand wird als Post-Lungenembolie-Syndrom bezeichnet.
Eine seltene Folge einer Lungenembolie ist die sogenannte chronisch thromboembolische Lungenerkrankung (CTEPD). Wie es dazu kommt, ist nicht genau bekannt. Man geht davon aus, dass sich das Blutgerinnsel in der Lunge nicht vollständig aufgelöst hat und in Narbengewebe umgewandelt wird. Ist als Folge der Blutdruck in den Lungengefäßen dauerhaft erhöht, sprechen Fachleute von einer chronisch thromboembolischen pulmonalen Hypertonie (CTEPH). Eine ausgeprägte CTEPH belastet das Herz stark und kann ein Herzversagen auslösen.
Die Symptome einer CTEPH sind unspezifisch – das heißt, sie können auch bei vielen anderen Erkrankungen auftreten. Eine CTEPH kann die gleichen Beschwerden wie eine Lungenembolie oder ein Post-Lungenembolie-Syndrom auslösen. Wenn einige Wochen oder Monate nach der Lungenembolie die körperliche Belastbarkeit abnimmt oder es sogar zu Atemnot und blutigem Auswurf kommt, ist es wichtig, die Ursache der Beschwerden rasch ärztlich abklären zu lassen.
Diagnose
Beschwerden wie plötzliche Schmerzen in der Brust oder Atemnot können auch andere Ursachen haben, etwa einen Herzinfarkt oder eine Lungenentzündung. Bei solchen Symptomen ist es immer wichtig, den Notruf 112 zu wählen, damit die Ursache schnell geklärt werden kann. Einem Verdacht auf Lungenembolie gehen die Ärztinnen und Ärzte in der Klinik sofort und systematisch nach, um im Fall einer schweren Embolie schnell handeln zu können. Welche Untersuchungen nötig sind, richtet sich insbesondere nach der
- Stabilität des Kreislaufs: Fachleute sprechen von einem instabilen Kreislauf, wenn der systolische Blutdruck über mindestens 15 Minuten weniger als 90 mmHg beträgt oder sehr stark abfällt. Andernfalls gilt der Kreislauf als stabil.
- Wahrscheinlichkeit für eine Lungenembolie: Diese hängt zum Beispiel davon ab, ob der Herzschlag beschleunigt ist, man vor kurzem operiert wurde oder eine tiefe Venenthrombose oder Krebserkrankung hat. Eine Rolle spielt auch, ob das Herz besonders belastet oder vorgeschädigt ist.
Häufig sind für die Diagnose viele aufeinander aufbauende Untersuchungen erforderlich.
Bluttest (D-Dimer-Test)
Der D-Dimer-Test reagiert auf Spaltprodukte, die der Körper produziert, wenn er ein Blutgerinnsel abbaut. Sie werden D-Dimere genannt. Ist der Test bei Personen mit stabilem Kreislauf und geringer Wahrscheinlichkeit für eine Lungenembolie unauffällig, lässt sich diese ziemlich sicher ausschließen. Wenn nicht, ist ein bildgebendes Verfahren notwendig, um die Diagnose zu bestätigen.
Bildgebende Verfahren
Eine Ultraschalluntersuchung (Sonografie) der Beinvenen kann sich anschließen. Wenn dabei eine Thrombose sichtbar wird, gilt die Lungenembolie als bestätigt. Andernfalls sind weitere Untersuchungen nötig. Weil der Ultraschall ohne Strahlung auskommt, eignet er sich besonders für schwangere Frauen.
Eine Ultraschalluntersuchung des Herzens (Echokardiografie oder Herzecho) kann zudem zeigen, wie stark die rechte Herzkammer belastet ist. Die weiteren bildgebenden Verfahren sind mit einer Belastung durch Strahlung und ein Kontrastmittel verbunden. Daher kommen sie nur infrage, wenn die Ärztinnen und Ärzte eine Lungenembolie für sehr wahrscheinlich halten. Bei Menschen mit instabilem Kreislauf werden sie für eine rasche Abklärung sofort eingesetzt.
Die Computertomografie-Pulmonalis-Angiografie (CTPA) ist eine spezielle Röntgenuntersuchung. Damit das Blutgerinnsel in der Lunge erkennbar ist, wird vorher ein jodhaltiges Kontrastmittel in die Armvene gespritzt.
Die kombinierte Ventilations-Perfusions-Szintigrafie kommt manchmal infrage, wenn keine CTPA möglich oder wenn sie zu risikoreich ist – wie bei einer Schwangerschaft, Nierenerkrankung oder Allergie gegen das Kontrastmittel. Die Ventilations-Perfusions-Szintigrafie zeigt die Durchblutung und die Verteilung der Atemluft in der Lunge. Dazu wird eine schwach radioaktive Substanz in die Vene gespritzt und zusätzlich inhaliert.
Behandlung
Wie eine Lungenembolie behandelt wird, hängt vor allem davon ab, ob der Kreislauf stabil ist.
Stabiler Kreislauf
Man bleibt häufig einige Tage im Krankenhaus und erhält gerinnungshemmende Medikamente. Fachleute bezeichnen solche Mittel als Gerinnungshemmer oder Antikoagulanzien. Die Behandlung heißt Antikoagulation.
Die Medikamente hemmen die Blutgerinnung und verhindern, dass das Gerinnsel wächst oder neue Blutgerinnsel entstehen. Dann kann der Körper das bestehende Gerinnsel nach und nach abbauen. Die häufigsten Nebenwirkungen von Gerinnungshemmern sind Blutungen, vor allem im Magen-Darm-Trakt.
Auch bei stabilem Kreislauf kann sich der Zustand plötzlich verschlechtern. Wenn es Anzeichen für diese seltene Komplikation gibt, wird man sicherheitshalber einige Tage auf der Intensivstation überwacht.
Instabiler Kreislauf
Bei instabilem Kreislauf ist normalerweise eine Behandlung auf der Intensivstation nötig. Dort kommen verschiedene die Atmung und den Kreislauf unterstützende Maßnahmen zum Einsatz, wie Infusionen, maschinelle Beatmung und ergänzende Medikamente. Außerdem beginnt sofort eine Behandlung mit Gerinnungshemmern – meist noch bevor die Diagnose abgeschlossen ist.
Darüber hinaus wird geprüft, ob eine systemische Thrombolyse oder ein minimalinvasiver Eingriff zur Entfernung des Thrombus sinnvoll ist. Bei einer Thrombolyse werden Medikamente in eine Vene gespritzt, die das Blutgerinnsel in der Lunge auflösen sollen. Die Behandlung wird als systemisch bezeichnet, weil sie im ganzen Körper wirkt – im Gegensatz zu einer örtlichen (lokalen) Therapie. Die Thrombolyse kann jedoch größere innere Blutungen auslösen, insbesondere im Kopf. Deshalb kommt sie nicht für alle Menschen mit schwerer Lungenembolie infrage.
Wenn keine systemische Thrombolyse möglich ist, können Ärztinnen und Ärzte das Blutgerinnsel mechanisch zerstören oder absaugen. Dazu schieben sie einen dünnen, biegsamen Schlauch (Katheter) bis zur verstopften Lungenarterie vor. Über den Katheter kann in der Lunge zugleich ein gering dosierter gerinnungshemmender Wirkstoff freigesetzt werden (lokale Thrombolyse). Dieses kombinierte Verfahren nennen Fachleute kathetergestützte Thrombolyse.
Nach der Akutbehandlung
Nach einer Lungenembolie bleibt man meist einige Tage im Krankenhaus. Vor der Entlassung ist wichtig, dass der Kreislauf stabil bleibt und man mit den gerinnungshemmenden Medikamenten zurechtkommt. Bei einer leichten Lungenembolie ist es manchmal schon nach 1 oder 2 Tagen möglich, wieder nach Hause zu gehen.
Die gerinnungshemmenden Mittel werden über einen Zeitraum von mindestens drei Monaten angewendet. Eine längere Behandlung kann sinnvoll sein, um zukünftigen Lungenembolien vorzubeugen. Die Vor- und Nachteile lassen sich im Gespräch mit der Ärztin oder dem Arzt abwägen.
Leben und Alltag
Insbesondere eine schwere Lungenembolie ist ein einschneidendes Erlebnis, das Spuren hinterlässt. Die Angst vor einer weiteren Lungenembolie begleitet dann oft das weitere Leben. Manchen Menschen hilft es, die gewohnte tägliche Routine wieder aufzunehmen, die Struktur und etwas Sicherheit gibt.
Körperliche Zeichen wie ein erhöhter Herzschlag oder Atemprobleme, die an die Lungenembolie erinnern, können besonders beängstigend sein. Deshalb trauen sich manche Menschen nach einer Lungenembolie nicht mehr, stärker körperlich aktiv zu sein. Einigen gelingt es jedoch, sportbedingte von krankheitsbedingten Symptomen zu unterscheiden.
Über solche Ängste und Erfahrungen zu sprechen, kann erleichternd sein. Dazu kann man sich einer Selbsthilfegruppe anschließen oder psychologische Unterstützung suchen, um besser mit der Angst zurechtzukommen.
Weil die gerinnungshemmende Behandlung schwere Blutungen auslösen kann, stehen ihr manche Menschen zunächst mit gemischten Gefühlen gegenüber. Einige stellen ihren Lebensstil um und meiden beispielsweise verletzungsträchtige Aktivitäten, um ihr Blutungsrisiko zu verringern.
Energielosigkeit oder Erschöpfung nach einer Lungenembolie können den Alltag zusätzlich beeinträchtigen. Seelisch belastend ist dann auch die Ungewissheit, wie lange dieser Zustand anhält. Ein Weg, mit den Nachwirkungen einer Lungenembolie umzugehen, kann sein, sich insgesamt weniger vorzunehmen oder Aufgaben in kleineren Schritten zu erledigen.
Bei jungen Menschen stellt eine Lungenembolie das Leben in besonderem Maße auf den Kopf. Viele werden sich der eigenen Verletzlichkeit bewusst. Einige fühlen sich „anders“ und vor allem gegenüber Gleichaltrigen ausgegrenzt. Auf Alkohol zu verzichten, weil sich die Medikamente nicht damit vertragen, kann in jungen Jahren besonders schwerfallen. Auch die tägliche Anwendung von Gerinnungshemmern ist für viele Jugendliche belastend.
Weitere Informationen
Die Hausarztpraxis ist meist die erste Anlaufstelle, wenn man krank ist oder bei einem Gesundheitsproblem ärztlichen Rat braucht. In unserem Thema „Gesundheitsversorgung in Deutschland“ informieren wir darüber, wie man die richtige Praxis findet – und mithilfe unserer Frageliste möchten wir dabei helfen, sich auf den Arztbesuch vorzubereiten.
Welche Gerinnungshemmer werden bei einer Lungenembolie angewendet?
Die folgenden gerinnungshemmenden Medikamente können zur Behandlung einer akuten Lungenembolie angewendet werden:
| Gerinnungshemmer | Anwendung | Regelmäßige Blutabnahme nötig | Besonderheiten |
|---|---|---|---|
| Heparin Es gibt niedermolekulares Heparin (NMH) und hochmolekulares oder unfraktioniertes Heparin (UFH). Gewöhnlich kommt NMH zum Einsatz. |
Spritze unter die Haut oder Spritze in eine Vene | bei niedermolekularem Heparin nein |
|
| Fondaparinux | Spritze unter die Haut | nein |
|
| Vitamin-K-Antagonisten, auch Cumarine genannt, wie Warfarin und Phenprocoumon („Marcumar“ oder "Falithrom"). | Tablette | ja |
|
| direkte orale Antikoagulanzien (DOAKs) wie Apixaban („Eliquis“), Edoxaban („Lixiana“), Rivaroxaban („Xarelto“) und Dabigatran („Pradaxa“) | Tablette | nein |
|
Eine akute Lungenembolie wird in den ersten Tagen oft mit Heparin behandelt. Wenn sich der gesundheitliche Zustand stabilisiert hat, wird die Behandlung in der Regel mit direkten oralen Antikoagulanzien, kurz DOAKs, fortgesetzt. Alternativ können bestimmte DOAKs auch von Anfang an, also ohne vorherige Behandlung mit Heparin, eingesetzt werden. Die Behandlung kann nach den ersten Tagen auch mit einem Vitamin-K-Antagonisten fortgesetzt werden.
Warum werden direkte orale Antikoagulanzien häufig bevorzugt?
Vitamin-K-Antagonisten (auch Cumarine genannt) waren lange die Standardbehandlung bei einer Lungenembolie. Sie haben aber auch Nachteile, zum Beispiel Wechselwirkungen mit zahlreichen anderen Medikamenten. Deshalb kommen sie nicht für alle Menschen mit Lungenembolie infrage.
Es ist außerdem nicht einfach, Vitamin-K-Antagonisten richtig zu dosieren. Deshalb ist es notwendig, die gerinnungshemmende Wirkung regelmäßig zu kontrollieren. Das bedeutet, dass regelmäßig Blut abgenommen werden muss. Weil Vitamin-K-Antagonisten die Blutgerinnung nicht direkt, sondern über einen Umweg hemmen, dauert es zudem einige Tage, bis sie wirken. Sie werden deshalb anfangs mit Heparin oder Fondaparinux kombiniert.
Direkte orale Antikoagulanzien (DOAKs) hemmen die Blutgerinnung im Gegensatz zu Vitamin-K-Antagonisten direkt. Sie sind einfach zu dosieren und es sind keine regelmäßigen Blutabnahmen nötig, um die gerinnungshemmende Wirkung zu kontrollieren. Die Mittel werden als Tablette in einer festen Dosierung eingenommen, und es reicht aus, diese hin und wieder zu prüfen. Außerdem haben DOAKs weniger Wechselwirkungen.
Insgesamt hängt die Wahl des Gerinnungshemmers vor allem davon ab, ob und welche weiteren Erkrankungen bestehen. Zusätzlich spielen Faktoren wie eine möglichst einfache Anwendung eine Rolle. Schwangere erhalten immer ein niedermolekulares Heparin, weil es nicht über die Plazenta an das ungeborene Kind weitergegeben wird.
Wie gut wirken Gerinnungshemmer?
Gerinnungshemmer wie Heparin, Fondaparinux, Vitamin-K-Antagonisten und DOAKs sind bei einer Lungenembolie gut wirksam. Sie können die Beschwerden der Lungenembolie lindern und Komplikationen vorbeugen. Die neueren DOAKs schnitten in Studien nicht schlechter ab als Vitamin-K-Antagonisten oder Heparin, die seit vielen Jahren zum Einsatz kommen.
Die gerinnungshemmenden Mittel werden über einen Zeitraum von mindestens drei Monaten angewendet. Danach wird abgewogen, ob eine längere Anwendung sinnvoll ist, um zukünftigen Lungenembolien vorzubeugen.
Welche Nebenwirkungen und Komplikationen sind möglich?
Ein Nachteil ist allen Gerinnungshemmern gemeinsam: Sie fördern Blutungen. Wer sie einnimmt, kann Blutungen mit verschiedenen Maßnahmen vorbeugen oder sie früh erkennen. Dazu gehört, auf Blut im Stuhl, Blutergüsse oder starkes Nasenbluten zu achten. Außerdem ist es sinnvoll, das Ärzteteam vor einem operativen Eingriff über die gerinnungshemmende Behandlung zu informieren, damit die Medikamente rechtzeitig abgesetzt werden können.
Starke Blutungen sind eine seltene, aber ernsthafte Komplikation der Gerinnungshemmer. Sie müssen rasch behandelt werden. In den ersten Wochen der Behandlung ist das Blutungsrisiko am höchsten.
Das Risiko für eine schwere Blutung steigt mit zunehmender Dosierung der Gerinnungshemmer. Weitere Risikofaktoren sind ein höheres Alter oder die gleichzeitige Anwendung anderer gerinnungshemmender Medikamente, zum Beispiel Acetylsalicylsäure (ASS), Clopidogrel oder nicht steroidale Antirheumatika (NSAR) wie Ibuprofen. Auch eine chronische Nieren- oder Lebererkrankung, eine Blutgerinnungsstörung oder Krebs fördern Blutungen.
Es ist sinnvoll, einen Medikamentenpass mit sich zu führen. Das ist ein kleines Heftchen oder Kärtchen mit der Information, welche Gerinnungshemmer in welcher Dosierung eingenommen werden. So ist in Notfällen – etwa bei Verletzungen oder Unfällen – schnell ersichtlich, was beachtet werden muss.
Erfahrungsberichte
Mehr Wissen
Extras
Quellen
Arbjerg Højen A, Dreyer PS, Lane DA et al. Adolescents' and Young Adults' Lived Experiences Following Venous Thromboembolism: "It will always lie in wait". Nurs Res 2016; 65(6): 455-464.
Crawford F, Andras A, Welch K et al. D-dimer test for excluding the diagnosis of pulmonary embolism. Cochrane Database Syst Rev 2016; (8): CD010864.
Deutsche Gesellschaft für Angiologie – Gesellschaft für Gefäßmedizin (DGA). Diagnostik und Therapie der Venenthrombose und der Lungenembolie (S2k-Leitlinie). AWMF-Registernr.: 065-002. 2015.
Duffett L, Castellucci LA, Forgie MA. Pulmonary embolism: update on management and controversies. BMJ 2020; 370: m2177.
Hao Q, Dong BR, Yue J et al. Thrombolytic therapy for pulmonary embolism. Cochrane Database Syst Rev 2018; (12): CD004437.
Izcovich A, Criniti JM, Popoff F et al. Thrombolytics for venous thromboembolic events: a systematic review with meta-analysis. Blood Advances 2020; 4(7): 1539-1553.
Khatib R, Ross S, Kennedy SA et al. Home vs hospital treatment of low-risk venous thromboembolism: a systematic review and meta-analysis. Blood Adv 2020; 4(3): 500-513.
Kirchberger I, Ruile S, Linseisen J et al. The lived experience with pulmonary embolism: A qualitative study using focus groups. Respir Med 2020; 167: 105978.
Konstantinides SV, Meyer G, Becattini C et al. 2019 ESC Guidelines for the diagnosis and management of acute pulmonary embolism developed in collaboration with the European Respiratory Society (ERS). Eur Heart J 2020; 41(4): 543-603.
Maughan BC, Frueh L, McDonagh MS et al. Outpatient Treatment of Low-risk Pulmonary Embolism in the Era of Direct Oral Anticoagulants: A Systematic Review. Acad Emerg Med 2021; 28(2): 226-239.
Noble S, Lewis R, Whithers J et al. Long-term psychological consequences of symptomatic pulmonary embolism: a qualitative study. BMJ Open 2014; 4(4): e004561.
Ortel TL, Neumann I, Ageno W et al. American Society of Hematology 2020 guidelines for management of venous thromboembolism: treatment of deep vein thrombosis and pulmonary embolism. Blood Adv 2020; 4(19): 4693-4738.
Pöss J, Freund A, Vollert JO et al. Lungenarterienembolie. Prozessorientierte und standardisierte Umsetzung der nationalen und internationalen Leitlinien. Kardiologe 2018; 12: 68–82.
Pschyrembel Online. 2022.
Robertson L, Kesteven P, McCaslin JE. Oral direct thrombin inhibitors or oral factor Xa inhibitors for the treatment of pulmonary embolism. Cochrane Database Syst Rev 2015; (12): CD010957.
Rolving N, Brocki BC, Andreasen J. Coping with everyday life and physical activity in the aftermath of an acute pulmonary embolism: A qualitative study exploring patients' perceptions and coping strategies. Thromb Res 2019; 182: 185-191.
Yoo HH, Nunes-Nogueira VS, Fortes Villas Boas PJ et al. Outpatient versus inpatient treatment for acute pulmonary embolism. Cochrane Database Syst Rev 2019; (3): CD010019.
Young T, Sriram KB. Vena caval filters for the prevention of pulmonary embolism. Cochrane Database Syst Rev 2020; (10): CD006212.